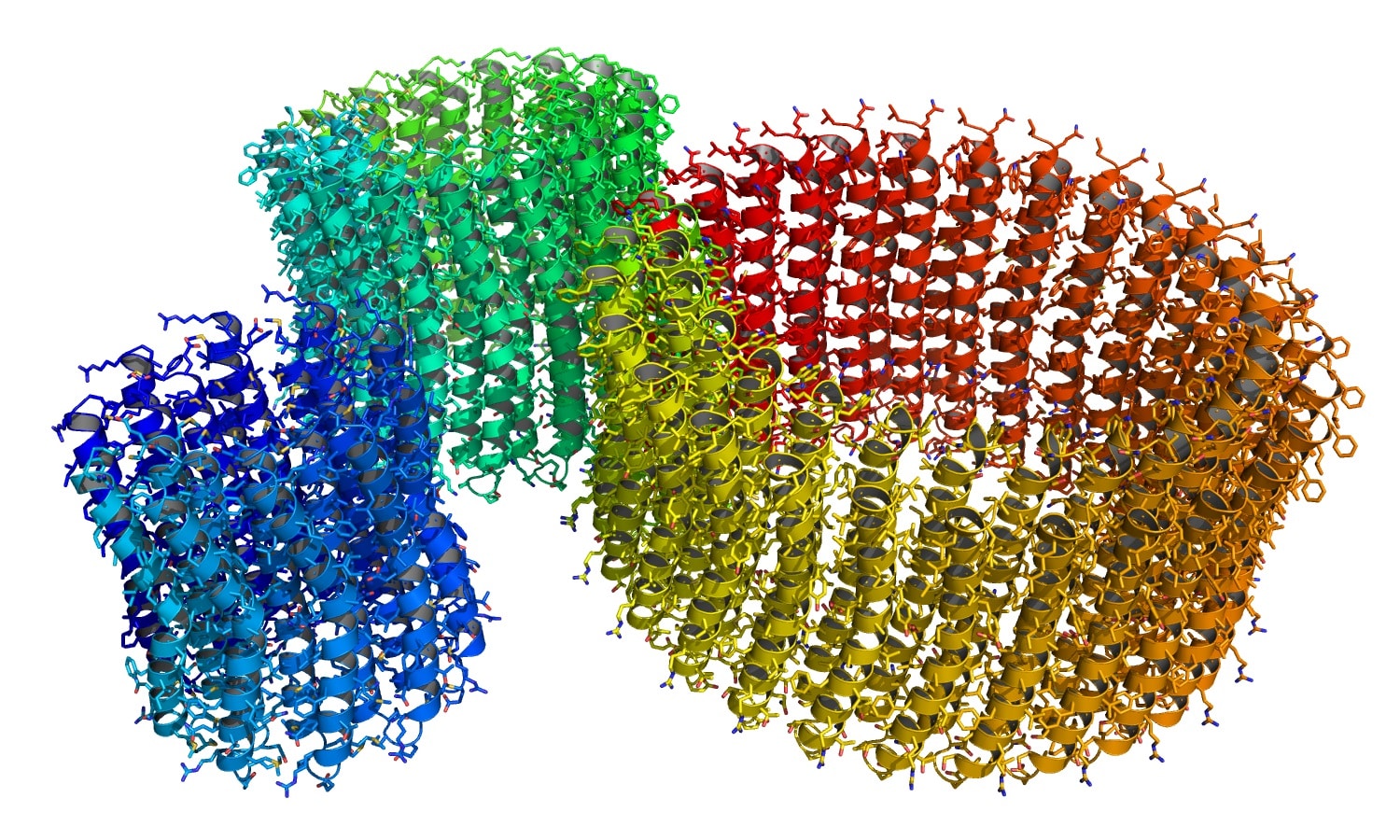
Группа ученых опубликовала результаты инновационного исследования в престижном журнале PROTEINS: Structure, Function, and Bioinformatics. В центре внимания оказалась АТФ-синтаза — удивительный молекулярный механизм, который можно назвать настоящей энергетической станцией живых организмов. Этот уникальный белковый комплекс преобразует мембранный потенциал в молекулы АТФ, служащие универсальным источником энергии для всех биологических процессов. Принцип работы АТФ-синтазы напоминает миниатюрный электродвигатель, где статор выступает неподвижной частью, а ротор (с-кольцо) совершает вращательные движения. При прохождении ионов через мембрану происходит вращение ротора, что обеспечивает синтез АТФ благодаря работе статора.
Современная наука располагает данными об АТФ-синтазах с различным количеством с-субъединиц — от 8 до 17. Традиционно их структуру изучали с помощью рентгеновской кристаллографии и крио-электронной микроскопии. Настоящий прорыв произошел благодаря развитию искусственного интеллекта и появлению программы AlphaFold, создатели которой были отмечены Нобелевской премией по химии в 2024 году. Однако стандартная версия AlphaFold имела ограничения при работе с крупными белковыми комплексами.
Специалисты МФТИ разработали инновационную методику на базе AlphaFold, которая позволяет с высокой точностью определять число субъединиц в белковых комплексах, обладающих вращательной симметрией. Точность предсказаний достигла впечатляющих 90% при сравнении с экспериментальными данными. Благодаря высокой скорости работы нового метода удалось проанализировать АТФ-синтазы широкого спектра живых организмов.
Исследование принесло удивительные результаты: была предсказана возможность существования микроорганизмов с АТФ-синтазами, содержащими до 27 субъединиц в с-кольце, что значительно превышает ранее известный максимум в 17 субъединиц. Достоверность этих предсказаний подтверждается компьютерным моделированием методом молекулярной динамики.
Возникает интригующий вопрос о целесообразности таких масштабных структур, учитывая эффективность более компактных роторов. Исследователи предполагают, что подобные организмы могут обитать в экстремальных условиях — при высоких температурах или в агрессивных средах с постоянной потерей ионов через мембраны. Также возможно, что большое количество субъединиц помогает компенсировать низкий энергетический потенциал на мембране, позволяя более эффективно улавливать редкие ионы. Хотя такие роторы расходуют больше протонов за оборот, они способны синтезировать АТФ при существенно меньших трансмембранных потенциалах.
Открытие открывает захватывающие перспективы в биотехнологии. Появляется возможность создавать молекулярные механизмы с заданными характеристиками, оптимизировать энергетический обмен в клетках и разрабатывать микроорганизмы, способные функционировать в экстремальных условиях, где обычные формы жизни не выживают.
Исследование демонстрирует огромный потенциал применения искусственного интеллекта и машинного обучения в современной структурной биологии. Оно не только расширяет возможности поиска новых белков в геномных данных, но и открывает путь к созданию белков с заранее заданными свойствами.
Проект реализован при поддержке Российского научного фонда и Министерства науки и высшего образования России.
Источник: naked-science.ru